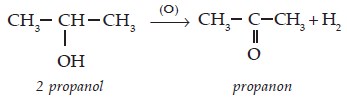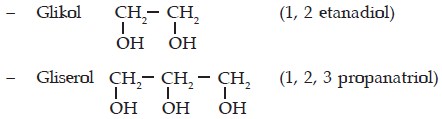Tata Nama Alkanol, Jenis-jenis, Sifat dan Kegunaan Alkanol
Alkanol atau Alkohol – Dalam senyawa karbon turunan alkana dimana dikenal senyawa yang biasanya disebut dengan alkohol dan eter. Alkohol dan eter merupakan isomer, karena memiliki rumus molekul yang sama yaitu CnH2n+2O. Namun kali ini kami ingin berbagi penjelasan khusus mengenai senyawa alkohol. Alkohol yang dikenal dalam kehidupan sehari-hari misalnya etanol yang merupakan salah satu anggota deret homolog alkohol. Alkohol merupakan golongan senyawa dengan rumus umum R – OH, di mana R adalah alkil (R = CnH2n+1). Dengan demikian alkohol dapat dianggap sebagai turunan dari alkana (R – H) di mana 1 atom H nya diganti dengan gugus – OH.
Alkanol
Oleh karena alkohol dianggap sebagai turunan dari alkana, maka alkohol diberi nama seperti alkana, hanya akhiran ana diganti dengan akhiran anol. Sehingga alkohol disebut juga dengan Alkanol. Jadi dalam pembahasan ini alkohol yang dimaksud sama dengan Alkanol.
Berikut gambaran bahwa alkohol/alkanol merupakan turunan dari alkana:
 |
| Alkanol atau Alkohol turunan Alkana |
Tata Nama Alkohol/Alkanol
a) Alkohol/Alkanol yang sudah berisomer, diberi nama dengan cara:
Menyebutkan nomor atom C yang mengikat OH kemudian nama alkanol (pengertian nomor dimulai dari atom C yang dekat dengan – OH).
Contoh:
b) Alkohol/Alkanol yang bercabang diberi nama dengan cara:
Menyebutkan nomor cabang, nama cabang, letak OH, dan nama alkanol rantai utama (atom C yang mengikat OH diberi nomor serendah mungkin).
Contoh:
Jenis-Jenis Alkohol/Alkanol
Berdasarkan letak gugus – OH, alkohol dibedakan menjadi 3 macam,
yaitu:
a) Alkohol/Alkanol Primer
Alkohol primer adalah alkohol yang gugus-OH nya terikat pada atom C primer (atom C yang terikat pada satu atom C lain).
Contoh: CH3 – CH2 – OH dan CH3 – CH2 – CH2 – OH
b) Alkohol/Alkanol Sekunder
Alkohol sekunder adalah alkohol yang gugus-OH nya terikat pada atom C sekunder.
Contoh:
c) Alkohol/Alkanol Tersier
Alkohol tersier adalah alkohol yang gugus-OH nya terikat pada atom tersier.
Contoh:
Gugus fungsional alkohol (– OH) dapat diidentifikasi dengan mereaksikannya dengan logam natrium yang menghasilkan gas hidrogen.
Reaksi: 2R – OH + 2Na → 2R – ONa + H2
Isomer Alkohol/Alkanol
Di kelas X, Anda telah mempelajari isomer rangka pada alkana, alkena, dan alkuna serta isomer geometri pada alkena (Jika sahabat dapat mempelarinya kembali). Alkohol selain memiliki isomer rangka juga memiliki isomer posisi dan isomer fungsi. Isomer fungsi, yaitu isomer yang disebabkan karena perbedaan posisi/letak gugus fungsi.
Contoh:
Isomer fungsi adalah isomer yang disebabkan oleh perbedaan gugus fungsi.
Misal: alkohol berisomer fungsi dengan eter.
Contoh: isomer C4H10O atau C4H9OH
Selain isomer-isomer di atas, alkohol sekunder yang mengandung atom C asimetris (atom C kiral) menunjukkan keisomeran optis. Atom C asimetris adalah atom C yang mengikat empat atom atau gugus yang berbeda.
Contoh:
Keisomeran optis berkaitan dengan sifat optis. Senyawa yang memiliki isomer optis dapat memutar bidang polarisasi cahaya dan disebut senyawa optis aktif. Senyawa yang mengandung 1 atom C kiral (misalnya 2 butanol) mempunyai 2 bentuk konfigurasi di mana bentuk yang satu merupakan bayang cermin dari yang lain. Dua isomer yang merupakan bayangan cermin satu dengan yang lainnya disebut enantiomer. Apabila berkas cahaya terpolarisasi dilewatkan melalui larutan yang mengandung enantiomer 2 butanol, bidang polarisasi akan terputar 13,52° ke kanan dan satu lagi memutar 13,52° ke kiri.
Sifat-Sifat Alkohol/Alkanol
a) Sifat Fisika
- Mempunyai titik didih lebih tinggi dari eter. Hal ini disebabkan antara molekul alkohol terjadi ikatan hidrogen.
- Metanol, etanol, dan propanol mudah larut, alkohol lainnya hanya sedikit larut.
b) Sifat Kimia
(1) Dapat bereaksi dengan logam (Na, K, Mg, Al) melepas H2.
Contoh: CH3 – CH2 – OH + Na → CH3 – CH2 – ONa + 1/2 H2
etanol natrium etanolat
(2) Dengan asam karboksilat membentuk ester (reaksi esterifikasi).
Secara umum:
Contoh: CH3 – CH2 – OH + PCl3 → CH3 – CH2 – Cl + H2O
etanol etil klorida
(4) Dengan asam halida (HX) membentuk alkil halida
Contoh: CH3 – CH2 – OH + HCl → CH3 – CH2 – Cl + H2O
etanol etil klorida
(5) Dapat Dioksidasi
- Oksidasi alkohol primer menghasilkan asam karboksilat.
- Oksidasi alkohol sekunder menghasilkan alkanon.
- Alkohol tersier tidak dapat dioksidasi.
Reaksi oksidasi alkohol ini dapat digunakan untuk membedakan alkohol primer, sekunder, dan tersier selain dengan reaksi Lucas (Reaksi antara alkohol dengan HCl).
- Alkohol primer + HCl → sangat lambat.
- Alkohol sekunder + HCl → cepat.
- Alkohol tersier + HCl → sangat cepat.
(6) Dapat mengalami dehidrasi dengan H2SO4 pekat.
- Pada suhu 140° C menghasilkan eter

- Pada suhu 180°C menghasilkan alkena
Polialkohol
Polialkohol/alkohol polivalen adalah alkohol yang memiliki lebih dari satu gugus – OH.
Contoh:
Pembuatan Alkohol/Alkanol
a) Metanol (CH3OH)
Metanol dibuat dengan cara hidrogenasi gas CO pada suhu 400°C dan tekanan 200 atm dengan katalisator Cr2O3 atau ZnO.
b) Etanol (C2H5OH)
Dalam bidang industri, etanol dibuat dengan fermentasi tetes tebu yaitu cairan gula yang tidak mengkristal/menghablur menjadi gula. Untuk memperoleh etanol pekat dilakukan destilasi/penyulingan.
c) Glikol (CH2OH CH2OH)
Glikol dibuat dengan cara mengoksidasi etana dengan oksigen kemudian dilanjutkan hidrolisis. Reaksi dilakukan pada suhu 250°C dengan katalisator serbuk perak.
d) Gliserol (CH2OH – CH2 OH CH2OH)
Gliserol diperoleh dari hasil samping pada pembuatan sabun.
Kegunaan dan Dampak Alkohol/Alkanol
a) Metanol
- Metanol digunakan untuk membuat metanol sebagai bahan plastik.
- Metanol digunakan untuk pelarut dan bahan pembuat ester, serta bahan bakar alternatif.
Di samping kegunaan metanol, terdapat dampak dari penggunaan metanol, yaitu sangat beracun. Keracunan metanol dapat melalui pernapasan (menghirup uapnya) dan dapat melalui kulit.
b) Etanol
Etanol digunakan sebagai pelarut, desinfektan, bahan pembuatan ester dan sebagai bahan bakar (di Brasil telah banyak kendaraan dengan bahan bakar etanol). Minuman beralkohol menimbulkan dampak negatif antara lain metanol menyebabkan mabuk dan mengantuk karena menekan aktivitas otak. Selain itu etanol bersifat adiktif yaitu menyebabkan kecanduan atau ketagihan, sehingga bila minum minuman beralkohol sulit untuk meninggalkan, padahal minum minuman beralkohol dilarang oleh agama dan pemerintah.
c) Glikol
Pada negara atau daerah bermusim dingin, glikol digunakan untuk zat anti beku pada radiator mobil. Glikol juga digunakan sebagai bahan baku dalam industri serat sintesis dan pelarut.
d) Gliserol
Gliserol digunakan untuk pelarut obat-obatan, dan bahan pembuatan gliserol trinitrat yaitu suatu bahan peledak.
Baca juga: Tekanan Osmotik Larutan Nonelektrolit.Demikian penjelasan mengenai Alkanol atau Alkohol mulai dari tata nama, jenis-jenis, isomer, sifat-sifat, pembuatan, sampai dengan kegunaan dan dampak dari alkohol/alkanol ini. Semoga penjelasan di atas dapat dipahami dan menjadi salah satu referensi yang baik bagi kita semua.