Bagaimana Jika Alkana Direaksikan dengan Golongan Halogen
Bagaimana Jika Alkana Direaksikan dengan Golongan Halogen – Sahabat, kali ini rumuskimia.net akan mencoba menjawab sebuah pertanyaan yang mungkin sering di tanyakan dalam ilmu kimia,terutama di tingkatan sekolah menengah atas yaitu bagaimana jika alkana direaksikan dengan golongan halogen?
 |
| Bagaimana Jika Alkana Direaksikan dengan Golongan Halogen? |
Bagaimana Jika Alkana Direaksikan dengan Golongan Halogen?
Adapaun jawaban dari pertanyaan di atas yaitu apabila alkana direaksikan dengan golongan halogen akan mengalami reaksi substitusi membentuk senyawa haloalkana dan asam halida atau asil halida.
Nach untuk memahami lebih lanjut mengenai alkana dapat direaksikan dengan golongan halogen, perlu pemahaman mengenai alkana dan golongan halogen itu sendiri.
Alkana adalah senyawa hidrokarbon jenuh yang memiliki ikatan kovalen tunggal. Sedangkan halogen adalah nama unsur untuk golongan VIIA yaitu F, Cl, Br, dan I.
Salah satu sifat alkana adalah dapat mengalamai reaksi substitusi (pertukaran) dengan unsur halogen (F2, Cl2, Br2, dan I2) atau disebut pula reaksi pertukaran yaitu pertukaran antara atom hidrogen pada alkana dengan atom halogen yang akan membentuk senyawa baru yaitu haloalkana dan asam halida.
Contoh Alkana Direaksikan dengan Golongan Halogen
Contoh 1:
CH4 + Cl2 ---> CH3Cl + HCl (terjadi reaksi substitusi)
Pertukaran atom H dan atom Cl
Produk yang terbentuk adalah CH3Cl = senyawa haloalkana dan HCl = asam halida
Contoh 2:
C2H5 + F2 ---> C2H4F + HF (terjadi reaksi substitusi)
Pertukaran atom H dan atom F
Produk yang terbentuk adalah C2H4F = senyawa haloalkana dan HF = asam halida
Senyawa Haloalkana
Haloalkana (disebut pula sebagai halogenoalkana atau alkil halida) merupakan suatu kelompok senyawa kimia yang berasal dari alkana yang mengandung satu atau lebih halogen. Mereka adalah bagian dari kelas umum halokarbon, meskipun perbedaan tersebut tidak sering dilakukan.
Haloalkana banyak digunakan secara komersial dan, akibatnya, dikenal dengan banyak nama kimia dan komersial. Mereka digunakan sebagai penghambat api, pemadam kebakaran, zat pendingin, bahan pembakar, pelarut, dan farmasi.
Setelah digunakan secara luas dalam perdagangan, banyak halokarbon juga telah ditunjukkan sebagai bahan pencemar yang serius dan racun. Sebagai contoh, klorofluorokarbon telah terbukti menyebabkan penipisan ozon.
Lihat Selengkapnya: Pengertian, Tata Nama, Contoh Soal dan Kegunaan Haloalkana
Asam Halida atau Asil Halida
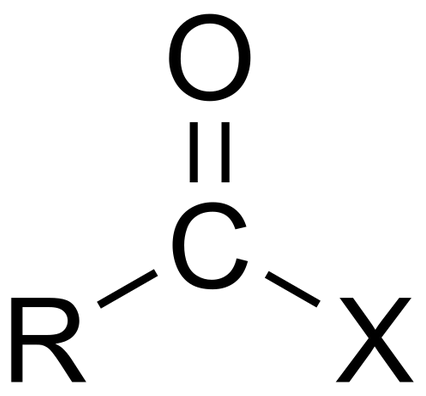 |
| Asam Halida atau Asil Halida |
Dalam kimia, istilah asam halida atau asil halida adalah suatu senyawa yang diturunkan dari sebuah asam karboksilat dengan menggantikan gugus hidroksil dengan gugus halida.
Jika asam tersebut adalah asam karboksilat, senyawa tersebut mengandung gugus fungsional -COX, yang terdiri dari gugus karbonil terikat pada atom halogen seperti pada klorin. Rumus umum untuk sebuah asil halida dapat dituliskan dengan RCOX, di mana R dapat sebuah gugus alkil, CO adalah gugus karbonil, dan X menunjukkan atom halogen.
Gugus RCO- adalah sebuah asil halida. Asil klorida adalah asil halida yang sering digunakan. Asil halida dibuat dengan halogenasi sebuah asam karboksilat, maka dari itu dinamakan asam halida. Jutaan kilogram senyawa ini diproduksi setiap tahunnya untuk memproduksi asam asetat.
Asil halida adalah senyawa buatan yang dibuat dalam reaksi tertentu dari senyawa organik lainnya. Asil halida dapat bereaksi dengan:
- air untuk membentuk asam karboksilat
- alkohol untuk membentuk ester
- amina untuk membentuk amida
- senyawa aromatik, menggunakan katalis AlCl3, untuk membentuk keton aromatik
- asam karboksilat untuk membentuk anhidrida asam.
Demikian jawaban dari pertanyaan bagaimana jika alkana direaksikan dengan golongan halogen? Semoga dapat dengan mudah dipahami dan memberikan manfaat bagi sahabat begitupun dengan kami.
Sumber:
Penulis Rumuskimia.net
Brainly (Akses 09 Februari 2022 jam 21.00)
Wikipedia (Akses 09 Februari 2022 jam 21.45)
Google Images